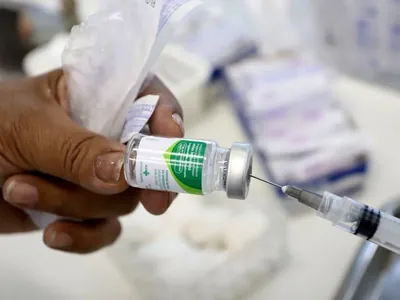
A Anvisa (Agência Nacional de Vigilância Sanitária) determinou nesta semana o recolhimento e a suspensão da venda de dois autotestes de covid-19 que haviam sido disponibilizados irregularmente para venda.
Os produtos que tiveram “o recolhimento e a suspensão da comercialização, distribuição, fabricação, importação, propaganda e uso” determinados são o “Autoteste Covid-19 Isa Lab” e o “Teste Covid meuDNA PCR-LAMP Autocoleta de Saliva”.
Em nota, a Anvisa reafirmou que, até o momento, não existe nenhum produto aprovado como autoteste, ou seja, para uso por usuários leigos.
“A Agência recebeu a denúncia em 20/1/2022 e encaminhou os casos com prioridade para investigação. Nessa etapa é avaliado o risco sanitário iminente à saúde da população e a medida restritiva tem o objetivo de reduzir o risco rapidamente”, informou a agência.
“Os casos seguem em avaliação e as infrações serão apuradas em processos administrativos próprios”, completou, ressaltando que disponibiliza um serviço de consulta a produtos irregulares.
Outro lado
Em notas, as empresas Isa Lab e Mendelics/meuDNA se pronunciaram sobre a decisão da Anvisa. Confira:
A Isa Lab informa que o kit citado no conteúdo da matéria trata-se de um teste de detecção de Covid-19 que utiliza como base do diagnóstico a técnica PCR-LAMP (Amplificação Isotérmica Mediada por Loop) a partir de uma amostra de saliva, que é coletada pelo próprio paciente. Portanto, trata-se de um teste de autocoleta e não um autoteste. Essa é uma maneira de testagem da infecção ativa, apontada pela Organização Mundial da Saúde (OMS) como a melhor ferramenta para rastrear o vírus e impedir a transmissão. Da mesma forma como acontece com o RT-PCR, o teste considerado “padrão ouro”, a técnica PCR-LAMP identifica o RNA do vírus nas células da pessoa infectada desde a fase inicial. E, apesar da amostra de saliva ser coletada pelo paciente, ela é encaminhada para a Mendelics, um laboratório de análises clínicas, líder em genômica no Brasil, devidamente registrado (CRM-SP 955.471) e acreditado (PALC 32290508, CGCRE Inmetro - Norma 15189:2015 - CLC 0007). É no laboratório que é realizada a análise e liberação de resultado.
A Isa Lab ressalta que o kit então comercializado está devidamente registrado na ANVISA sob o código de registro nº 10237610236 (autorização: 1.02.376-1) e está de acordo com a legislação e regulamentação vigentes. A embalagem do produto foi desenvolvida quando a categoria de autotestes ainda não se fazia uma realidade no mundo.
Por fim, até que haja uma reavaliação do entendimento da Anvisa quanto à suspensão presente, a Isa Lab retirou o produto de comercialização e reforça seu compromisso com a segurança e bem-estar dos clientes, que contam com um atendimento atestado pelo certificado ONA - uma metodologia de acreditação desenvolvida em 1999, a partir de métodos de certificação regionais da América Latina e de outros países, como Estados Unidos, Canadá, Espanha e Inglaterra, que tem por objetivo geral estimular o desenvolvimento de um processo permanente de avaliação e certificação da qualidade dos serviços de saúde.
Mendelics/meuDNA
Referente à resolução ANVISA (213/2022) datada de 25/01/2022, informamos:
1. O kit de coleta de saliva vendido em farmácias é um produto registrado na ANVISA sob o código de registro nº 10237610236 (autorização: 1.02.376-1) e está de acordo com a legislação e regulamentação vigentes. O kit de coleta de saliva é utilizado para autocoleta, da mesma maneira que kits de coleta de urina, escarro e fezes são utilizados para coletas domiciliares de amostras subsequentemente analisadas em laboratórios de análises clínicas.
2. O teste meuDNA Covid não se trata de um autoteste ou de teste rápido. Não há testagem realizada pelo paciente ou pelo farmacêutico. O teste meuDNA Covid é um teste laboratorial com fim diagnóstico, realizado no laboratório Mendelics. A Mendelics é um laboratório de análises clínicas, líder em genômica no Brasil, devidamente registrado (CRM-SP 955.471) e acreditado (PALC 32290508, CGCRE Inmetro - Norma 15189:2015 - CLC 0007). Os testes realizados pela Mendelics são regidos pela RDC 302/2005 da ANVISA.
3. O teste meuDNA disponível em farmácias e no site meudna.com utiliza como base do diagnóstico a técnica PCR-LAMP (Amplificação Isotérmica Mediada por Loop). Assim como o RT-PCR, o teste considerado "padrão ouro", ela identifica o RNA do vírus nas células da pessoa infectada desde a fase inicial. Ou seja, trata-se de uma maneira de testagem da infecção ativa, apontada pela Organização Mundial da Saúde (OMS) como a melhor ferramenta para rastrear o vírus e impedir a transmissão.
Em face de mais uma onda de Covid que assola o país e da falta de testes disponíveis em muitos locais, esperamos que a ANVISA reavalie esta interpretação errônea e libere novamente os kits de autocoleta de saliva meuDNA para comercialização nas farmácias PagueMenos o mais rápido possível.
Decisão sobre autoteste
No dia 19 de janeiro, diretores da Anvisa se reuniram para discutir a autorização e a viabilidade de comercialização ao consumidor de testes rápidos de antígeno para diagnóstico de covid-19, os chamados autotestes.
Alegando falta de informações e “lacunas” na documentação enviada pelo Ministério da Saúde, a decisão foi adiada.
O ministério liderado pelo ministro Marcelo Queiroga considera que o autoteste “pode ser uma excelente estratégia de triagem” e, pelo resultado rápido, deve “acelerar o início do isolamento dos casos positivos e as ações para interrupção da cadeia de transmissão”.
O principal problema técnico pontuado por profissionais da Anvisa seria a falta de uma política pública envolvendo o uso do autoteste. A agência teme que, com os diagnósticos feitos em casa, o Brasil enfrente uma subnotificação de casos confirmados de covid-19.
Nesta semana, o ministério enviou documentações complementares e uma nova decisão sobre o tema deve ser tomada nos próximos dias.